传统药物筛选长期依赖经验主义,科研人员从天然产物、化学合成库中随机选取化合物进行测试,效率低下且成本高昂。例如,青霉素的发现虽具里程碑意义,但其过程充满偶然性,耗费了弗莱明数年时间。随着分子生物学、计算科学的发展,药物筛选逐渐转向科学系统化。高通量筛选技术(HTS)的出现,使单日化合物测试量从数十种跃升至数万种,结合自动化液体处理系统、高内涵成像技术,可同步分析细胞活性、基因表达等多维度数据。计算机辅助药物设计(CADD)则通过分子对接、药效团模型等算法,在虚拟环境中预测化合物与靶点的结合能力,将筛选范围从实体化合物库扩展至“虚拟库”,明显提升发现效率。如今,药物筛选已形成“计算筛选-实验验证-优化迭代”的闭环体系,为新药研发奠定坚实基础。斑马鱼模型评价眼毒性。评价药物安全性
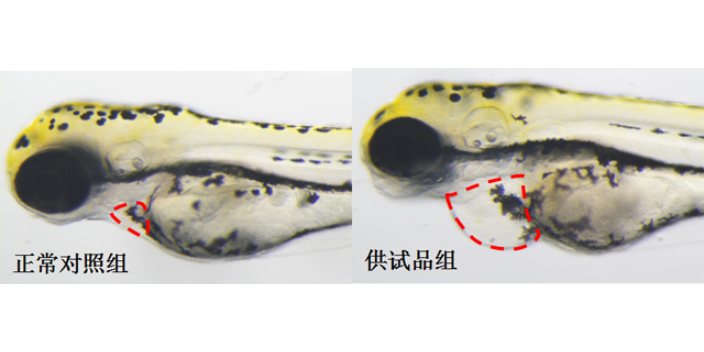
单一组学研究往往难以多方面揭示药物复杂的作用机理,多组学整合研究成为药品机理研究的新趋势。基因组学、转录组学、蛋白质组学和代谢组学等多组学数据的整合分析,能够从多个层面、系统地阐述药物与机体相互作用的机制。通过基因组学研究,可以了解药物作用相关的基因变异情况,为药物敏感性和个性化用药提供依据;转录组学分析药物处理后基因表达的变化,可发现药物调控的关键信号通路;蛋白质组学明确药物作用后蛋白质的变化,确定直接作用靶点;代谢组学则检测药物引起的代谢物变化,反映药物对机体代谢的影响。例如,在糖尿病药物机理研究中,整合多组学数据发现,某种药物不仅通过调节胰岛素分泌相关基因表达,还通过影响糖代谢关键酶的活性和代谢物水平,多途径发挥降低人体血糖作用。多组学整合研究突破了单一组学的局限性,为深入理解药物作用机理、发现新的药物作用机制和医疗靶点提供了多方面的视角。体外活性评价 药物研发利用斑马鱼模型评价降尿酸功效。
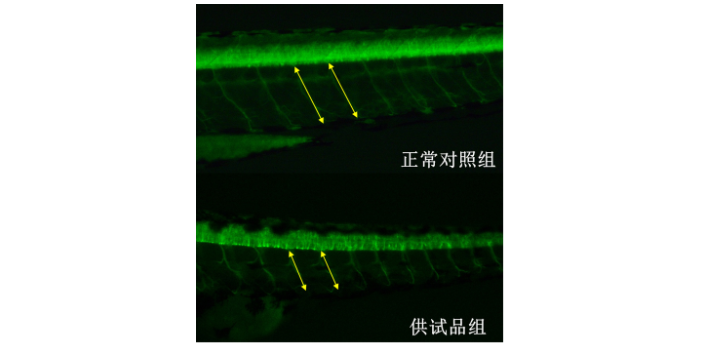
中药药效评价需结合体内外实验模型,验证其医疗作用。体外实验常用细胞模型,如人肝ancer细胞HepG2用于评估中药抗tumor活性。例如,研究发现黄连素可通过诱导细胞凋亡抑制肝ancer细胞增殖。体内实验则依赖动物模型,如糖尿病小鼠模型用于测试中药降糖效果。例如,六味地黄丸可明显降低糖尿病小鼠的空腹血糖和糖化血红蛋白水平。此外,网络药理学技术通过整合多组学数据,预测中药与靶点的相互作用,为实验设计提供方向。例如,通过构建“成分-靶点-疾病”网络,发现黄芪多糖可能通过调节PI3K/Akt信号通路发挥免疫调节作用。
原发性肝cancer(Primary Liver Cancer, PLC)是全球cancer相关死亡的第三大原因,包括肝细胞cancer(Hepatocellular Carcinoma, HCC)、肝内胆管cancer(Intrahepatic Cholangiocarcinoma, ICC)及混合型肝细胞-胆管cancer(Combined Hepatocellular-Cholangiocarcinoma, CHC)。内异质性(Intra-tumor Heterogeneity, ITH)被认为是cancer医疗的主要障碍。先前的研究已经揭示了HCC、ICC和CHC中存在相当程度的基因组异质性,反映了具有不同分子特征的多样化细胞群,决定了药物敏感性并可能导致医疗失败。患者来源的类organ(Patient-derived Organoids, PDO)培养已被证明是一种强大的工具,可以用于再现异质性并研究不同cancer类型中的药物敏感性,包括PLC疾病建模和药物筛选。然而,以前的PLC类organ研究受到样本数量的限制,且缺乏多区域样本。因此,建立一个大规模的PLC类organ生物库,对PLC异质性的深入理解和开发新的医疗策略,尤其对个性化医疗和精细医疗至关重要。斑马鱼模型评价半数致死浓度。
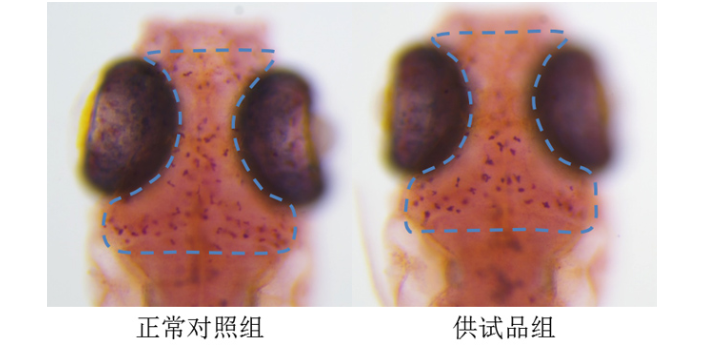
传统中药制剂存在生物利用度低、靶向性差等问题,而纳米技术的发展为其提供了解决方案。例如,将姜黄素负载于聚乳酸-羟基乙酸共聚物(PLGA)纳米粒中,其粒径控制在100-200nm,表面修饰转铁蛋白受体抗体后,可主动靶向脑肿瘤细胞。实验显示,该制剂在脑中的浓度较游离姜黄素提高8倍,且对正常细胞毒性降低60%。另一案例是青蒿素脂质体,通过磷脂双分子层包裹,其半衰期从2小时延长至12小时,抗疟活性提升3倍。此外,3D打印技术已用于制备个性化中药纳米贴片,通过控制药物释放速率,实现局部慢性病(如关节炎)的精细医疗。这些创新制剂,正重塑中药的给药的方式与疗效评价体系。药物高通量筛选、化合物活性筛选。药物的计量与药效关系实验
斑马鱼实验模型-药物、化妆品功效评价。评价药物安全性
中药对免疫系统的调节作用常涉及细胞因子网络的动态平衡。以雷公藤甲素为例,其可通过抑制NF-κB通路,下调TNF-α、IL-6等促炎因子,同时上调IL-10、TGF-β等抑炎因子,缓解类风湿关节炎症状。实验显示,雷公藤甲素处理后的佐剂性关节炎大鼠,其关节肿胀度较对照组降低60%。另一机制是中药对T细胞亚群的调节,如黄芪多糖可促进调节性T细胞(Treg)分化,抑制Th17细胞过度活化,维持免疫耐受。此外,中药复方(如玉屏风散)可通过调节肠道菌群,影响短链脂肪酸(如丁酸)产生,间接调节免疫细胞功能。这些细胞因子网络研究,为中药免疫调节提供了系统生物学视角。评价药物安全性