- 产地
- 苏州
- 品牌
- 外泌体提取试剂
- 型号
- 齐全
- 是否定制
- 是
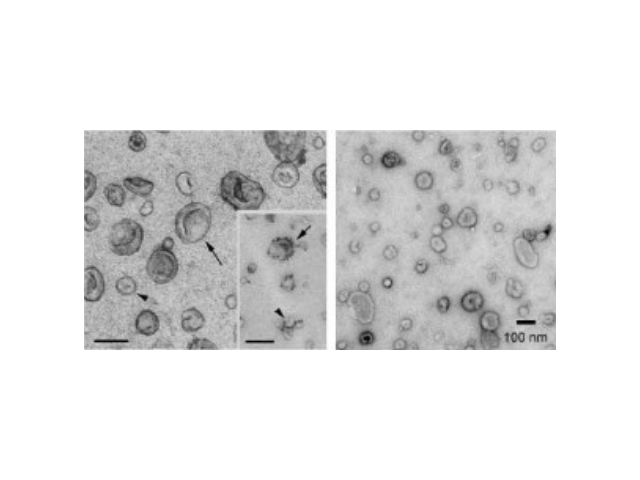
外泌体的形成与鉴定:首先,细胞膜内陷形成一个杯状结构,包括细胞表面蛋白和与细胞外环境相关的可溶性蛋白,导致早期胞内体(early-sortingendosome,ESE)的从头形成,或者是杯状结构直接和已经存在的ESEs融合;trans-高尔基体和内质网也能协助形成ESEs。ESE成熟后形成晚期胞内体(late-sortingendosomes,LSEs),较终形成MVBs(也称为多囊内小体)。MVBs是通过endosome限制膜向内凹(即质膜双凹)形成的,这一过程导致MVBs含有多个ILVs。MVB可以与溶酶体或自噬体融合,较终降解或与质膜融合释放作为外泌体的ILVs。外泌体表面蛋白包括四聚体蛋白、整合蛋白、免疫调节蛋白等。外泌体可以包含不同类型的细胞表面蛋白、细胞内蛋白、RNA、DNA、氨基酸和代谢物。使用可截留100KD分子量的膜,通过离心截留上清中的外泌体,截留完成后。外泌体的提取有超速离心、试剂盒、超滤法、蔗糖密度梯度离心等,然而各种方法均有其利弊。金华正规外泌体提取试剂供应商

在无菌条件下提取人体体液,并用PBS缓冲液进行稀释,然后通过离心筛选初步去除体液中的细胞成分和细胞碎片,制成体液样本备用;体液样本纯化:通过过滤膜对上述体液样本进行过滤,进一步去除体液中的细胞残片及其他杂质,静置10~15分钟,留取沉淀物备用;外泌体提取:将上述沉淀物用PBS缓冲液进行悬浮,使外泌体悬浮于液体上层,然后用无菌针管吸取上层含有外泌体的液体,置于80℃储存备用。此提取方法条件复杂,成本高,专利申请利用静置不太可能把外泌体沉降下来;根据外泌体表面的特异生物化学特性通过提取试剂的特异配方把外泌体从水相中沉降下来。不同细胞分泌的外泌体具有不用的组成成分和功能,可作为疾病诊断的生物标志物。温州正规外泌体提取试剂外泌体提取:聚乙二醇(PEG)为常用的多聚物,可与疏水性蛋白和脂质分子结合共沉淀。

外泌体的提取分离:1、PEG-base沉淀法。聚乙二醇(PEG)可与疏水性蛋白和脂质分子结合共沉淀,早先应用于从血清等样本中收集病毒,现在也被用来沉淀外泌体,其原理可能与竞争性结合游离水分子有关。利用PEG沉淀外泌体存在不少问题:比如纯度和回收率低,杂蛋白较多(假阳性),颗粒大小不均一,产生难以去除的聚合物,机械力或者吐温-20等化学添加物将会破坏外泌体等,因此发表文章时易受质疑。2、试剂盒提取。近几年来,市场上已出现各种商业化的外泌体提取试剂盒,有的是通过特殊设计的过滤器过滤掉杂质成分,有的则采用空间排阻色谱法(SEC)进行分离纯化,也有的则利用化合物沉淀将法外泌体沉淀出来。这些试剂盒不需要特殊设备,随着产品不断更新换代,提取效率和纯化效果逐渐提高,因而逐渐取代超速离心法并推广开来。有些试剂盒操作简便,不用超速离心,同时可获得高纯度和高回收率的外泌体。
外泌体相关miRNA与肺病的诊断:miRNAs是一类含有20~25个核苷酸的非编码小RNA,能够通过下调或压制靶mRNAs来调节转录水平上的基因表达,目前非编码RNA被普遍发现存在于NSCLC患者外泌体中,参与一些病症的形成和演化过程。单个miRNA可能通过压制性复合物与多个mRNA结合,从而阻滞整个生物通路。因此,外泌体的miRNA具有成为NSCLC标志物的优势。Chen等在152例肺病患者的研究中初次报道了循环游离miRNA的表达,与75例健康者相比,发现了两种高表达的miRNA(miR-25和miR-223)。Rabinonowits等对27例肺病患者和9例健康人的血浆外泌体中12个miRNA的表达进行了评估,结果显示,12个一些病症相关的miRNA*在肺病患者中过度表达。Cazzoli等收集了30个血浆样本,发现4种外泌体miRNA(miR-378a、-379a、-139-5p、-200b-5p)在肺病患者血清中明显升高,用于筛查患者与健康人ROC曲线下面积(AUC)为0.908。此提取方法条件复杂,成本高。

外泌体的提取主要包括以下几种方式:一是超速离心法,这是目前外泌体提取较常用的方法。此种方法得到的外泌体量多,但是纯度不足,电镜鉴定时发现外泌体聚集成块,由于微泡和外泌体没有非常统一的鉴定标准,也有一些研究认为此种方法得到的是微泡不是外泌体。二是过滤离心,这种操作简单、省时,不影响外泌体的生物活性,但同样存在纯度不足的问题。三是密度梯度离心法,用此种方法分离到的外泌体纯度高,但是前期准备工作繁杂,耗时,量少。四是免疫磁珠法,这种方法可以保证外泌体形态的完整,特异性高、操作简单、不需要昂贵的仪器设备,但是非中性pH和非生理性盐浓度会影响外泌体生物活性,不便进行下一步的实验。五是PS亲和法,该方法将PS(磷脂酰丝氨酸)与磁珠结合,利用亲和原理捕获外泌体囊泡外的PS。该方法与免疫磁珠法相似,获得的外泌体形态完整,纯度较高。由于不使用变性剂,不影响外泌体的生物活性,外泌体可用于细胞共培养和体内注射。2016.9《ScientificReports》杂志发表了该方法较新数据,表明PS法可提取相当高纯度的外泌体。六是色谱法,这种方法分离到的外泌体在电镜下大小均一,但是需要特殊的设备,应用不普遍。外泌体的提取方法,先用含无外泌体血清的培养基对人脂肪来源间充质干细胞进行饥饿培养。金华正规外泌体提取试剂供应商
专利申请利用分离培养人尿液来源细胞并收集培养基来进行体外培养。金华正规外泌体提取试剂供应商
外泌体的提取、分离方法:开发高效、快速、稳定,并且保持外泌体结构和生物功能完整性的方法,是目前外泌体应用于临床的基础和前提。从细胞上清和体液中提取分离外泌体的方法很多,但是外泌体的纯度和产量却和分离方法息息相关。通常分离步骤少、产率高,但是纯度会受到影响。鉴于每种分离方法都有其优缺点,实验可以根据样本来源、下游实验目的等,选择合适的外泌体分离方法。2015年,国际囊泡组织(InternationSocietyforExtracelluarVesicles,ISEV)指出,简单依靠一种分离方法得到的外泌体的纯度和产量都难满足实验的需求。因此,推荐联合使用各种方法,从而得到高纯度和高产量的外泌体。金华正规外泌体提取试剂供应商
外泌体的功能取决于其所来源的细胞类型,其可参与到机体免疫应答、抗原提呈、细胞迁移、细胞分化、一些病症侵袭等方方面面。有研究表明一些病症来源的外泌体参与到一些病症细胞与基底细胞的遗传信息的交换,从而导致大量新生血管的生成,促进了一些病症的生长与侵袭。功能:当外泌体在1980年初次被发现后,其被认为是细胞排泄废物的一种方式,如今随着大量对其生物来源、其物质构成及运输、细胞间信号的传导以及在体液中的分布的研究发现外泌体具有多种多样的功能。使用PBS对膜进行洗脱即得到外泌体浓缩液。上海正规外泌体提取试剂单价外泌体相关蛋白质与肺病的诊断:近年来,高通量质谱分析被普遍地应用于筛选NSCLC外泌体蛋白的研究...
- 北京外泌体提取试剂服务电话 2026-05-04
- 广州外泌体提取试剂进货价 2026-05-03
- 郑州外泌体提取试剂报价 2026-05-03
- 唐山正规外泌体提取试剂进货价 2026-05-03
- 上海外泌体提取试剂直销厂家 2026-05-02
- 徐州外泌体提取试剂价格 2026-05-02
- 广州外泌体提取试剂直销厂家 2026-05-02
- 太原正规外泌体提取试剂厂家直销 2026-05-01
- 芜湖外泌体提取试剂厂家批发价 2026-05-01
- 广州外泌体提取试剂价格 2026-04-30
- 济南外泌体提取试剂销售厂家 2026-04-29
- 温州正规外泌体提取试剂直销价 2026-04-29
- 开封正规外泌体提取试剂单价 2026-04-29
- 开封外泌体提取试剂直销价 2026-04-29
- 徐州正规外泌体提取试剂直销厂家 2026-04-29
- 济南外泌体提取试剂直销价 2026-04-29


- 成都细胞外基质胶厂家供应 05-04
- 正规细胞外基质胶哪家好 05-04
- 青岛细胞高效转染试剂服务电话 05-04
- 开封正规原代细胞分离试剂盒哪家便宜 05-04
- 开封细胞高效转染试剂厂家推荐 05-04
- 深圳细胞外基质胶供应商 05-04
- 南昌正规鼠尾胶原厂家直销 05-04
- 无锡太原RNA提取试剂 05-04
- 贵阳细胞高效转染试剂进货价 05-04
- 武汉细胞高效转染试剂推荐厂家 05-04