- 产地
- 苏州
- 品牌
- 细胞外基质胶
- 型号
- 齐全
- 是否定制
- 是
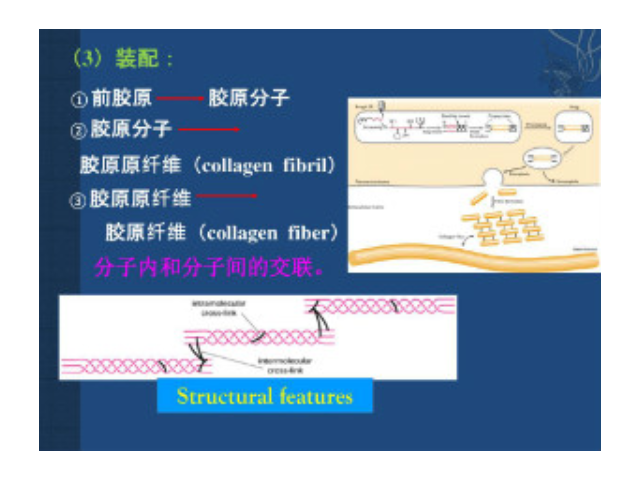
涉及纤连蛋白基质组装的信号传导途径:原纤维形成检测(货号:FNR01,FNR02,FNR03)与其他可以在生理条件下自动聚合的ECM组分不同,Fibronectin的组装是一种依赖细胞的过程。了解FN组装所涉及的机制以及这些与细胞,纤维化和免疫反应之间的相互作用可能揭示了调控异常组织修复过程的疗法的未来发展目标。同样,组织工程很大程度上依赖于控制细胞外基质形成的速率和模式的能力。Cytoskeleton荧光标记的Fibronectin可用于检测原纤维形成。荧光纤连蛋白(FNR01 和FNR02该方法涉及通过掺入荧光纤连蛋白来对纤维丝形成进行荧光示踪(17),通过向细胞培养基中加入TRITC标记的Fibronectin(FNR01)或HiLyte488标记的Fibronectin(FNR02),可以观察到可溶性Fibronectin向细胞表面不溶纤维丝的转化,掺入的纤连蛋白的水平可以通过荧光显微镜观察和定量(18)。微环境中的免疫细胞及因子又可以影响部位细胞的生长。杭州郑州细胞外基质胶
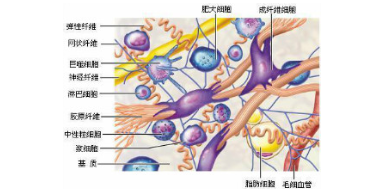
细胞外基质弹性蛋白:弹性蛋白纤维网络赋予组织以弹性,弹性纤维的伸展性比同样横截面积的橡皮条至少大5倍。弹性蛋白由二种类型短肽段交替排列构成。一种是疏水短肽赋予分子以弹性;另一种短肽为富丙氨酸及赖氨酸残基的α螺旋,负责在相邻分子间形成交联。弹性蛋白的氨基酸组成似胶原,也富于甘氨酸及脯氨酸,但很少含羟脯氨酸,不含羟赖氨酸,没有胶原特有的Gly-X-Y序列,故不形成规则的三股螺旋结构。弹性蛋白分子间的交联比胶原更复杂。通过赖氨酸残基参与的交联形成富于弹性的网状结构。无锡正规细胞外基质胶进货价系膜细胞病变克制了肾脏纤溶酶的降解活性。

细胞外基质与医学:目前学者们一致认为恶性部位的侵蚀、转移是一个动态的、连续的过程。部位细胞首先从原发部位脱落,侵入到细胞外基质(extracellular ma-tric,ECM),与基底膜(basement membrane,BM)与细胞间质中一些分子粘附,并启动细胞合成、分泌各种降解酶类,协助部位细胞穿过ECM进入血管,然后在某些因子等的作用下运行并穿过血管壁外渗到继发部位,继续增殖、形成转移灶。总之,脱落、粘附、降解、移动和增生贯穿于恶性部位侵蚀、转移的全过程。ECM由BM和细胞间质组成,为部位转移的重要组织屏障。部位细胞通过其表面受体与ECM中的各种成分粘附后启动或分泌蛋白降解酶类来降解基质,从而形成局部溶解区,构成了部位细胞转移运行通道。一般恶性程度高的部位细胞具有较强的蛋白水解作用,可侵蚀破坏包膜,促进转移。目前较为关注的酶主要是丝氨酸蛋白酶类,如纤溶酶原启动物(plasminogen activator,PA)和金属蛋白酶(metalproteinase,MP)类,如胶原酶IV、基质降解酶、透明质酸酶.。
细胞外基质偶联调控细胞单层的受力反应:上皮细胞在基底上因受弹性、边缘和界面三个效应的共同作用,可以形成形态丰富的粘着单层。细胞通过粘着斑感受其外界环境,可看作是细胞与基质之间的机械连接。之前的力生物学研究主要集中于单个细胞,而来自美国宾州大学的张宿林教授等却探索了多细胞的受力反应,探讨了单层细胞作为整体如何传递和分配牵引力。他们基于分子的热力学模型、单层-底物弹性的整合和力-介导的粘着形成,建立了热力学模型,提出了粘着形成机制,并通过显微观察牵引力作用等实验测量方法来验证该模型的预测结果。不同细胞具有不同的细胞外基质,介导的细胞骨架组装的状况不同。
蛋白聚糖在细胞外基质中的功能是什么: 蛋白聚糖或透明质酸-蛋白聚糖复合物构成了细胞外基质的基质,由于它们是高度酸性的,且带负电荷,因此能够结合大量的阳离子,这些阳离子又可结合大量的水分子,这样,蛋白聚糖形成了多孔的、吸水的胶状物,如同包装材料,填充在细胞外基质中。蛋白聚糖的这种性质,使细胞表面具有较大的可塑性,从而具有抗挤压能力,对细胞起保护作用。由于透明质酸以可溶的形式游离存在,所以在细胞外体液和滑液(synovialfluid)中透明质酸的浓度很高,其结果提高了体液和滑液的粘度和润滑性。单个的蛋白聚糖和透明质酸-蛋白聚糖复合物直接与胶原纤维连接形成动物细胞外的纤维-网络(fiber-network)结构,不同类型的胶原和不同类型的蛋白聚糖连接形成不同的纤维-网络,对于提高细胞外基质的连贯性起关键作用。此外,蛋白聚糖还可作为细胞粘着的暂时性或长久性的位点。暂时性的粘着发生在胚胎发育中,对于单个细胞及细胞层的移动具有重要作用。另外,蛋白聚糖对于细胞分化也十分重要,同时也与细胞变有关。主要是一些多糖和蛋白, 或蛋白聚糖。南昌正规细胞外基质胶产品介绍
在层粘连蛋白上则停止增殖,进行分化,融合为肌管。杭州郑州细胞外基质胶
细胞外基质粘弹性影响细胞行为:组织和细胞外基质的复杂力学行为,讨论了细胞外基质粘弹性对细胞的影响,并描述了粘弹性生物材料在再生医学中的潜在应用。生物材料设计历来没有考虑到粘弹性的重要性,但是展望未来,粘弹性很可能成为许多应用中的关键技术规范(如图5)。粘弹性在调节可能包括多能干细胞、组织驻留干细胞和分化细胞以及免疫细胞在内的各种细胞类型生物学调节中的作用,以便合理设计能够促进组织再生的材料。生物材料的设计也可能需要将细胞感知的局部粘弹性特性与实现再生或工程组织机械稳定性所需的更大的组织尺度特性相分离。因此,具有可控粘弹性的生物材料的出现可能会改变生物材料在再生医学中的应用。杭州郑州细胞外基质胶
细胞外基质这个名词主要指动物细胞的细胞外基质,植物细胞的细胞外是细胞壁。高等动物的组织有4大类:上皮组织、结缔组织、肌肉组织、神经组织,组织是细胞和细胞外基质的,所以细胞外基质也应该有4大类:上皮组织的细胞外基质、结缔组织的细胞外基质、肌肉组织的细胞外基质、神经组织的细胞外基质。由于结缔组织的细胞外基质的细胞外基质非常丰富,所以教科书上讲的细胞外基质的成分实际上是结缔组织的细胞外基质。细胞外基质可以控制细胞迁移的速度与方向,并为细胞迁移提供“脚手架”。胶原蛋白属于不溶性纤维形蛋白质,是细胞外基质的主要成分,遍布于各部位和组织。重庆正规细胞外基质胶厂家推荐细胞外基质弹性蛋白:弹性蛋白纤维网络赋予...
- 昆明细胞外基质胶厂家推荐 2026-05-19
- 温州正规细胞外基质胶厂家现货 2026-05-19
- 合肥昆明细胞外基质胶 2026-05-19
- 金华细胞外基质胶直销厂家 2026-05-18
- 唐山细胞外基质胶厂家直销 2026-05-18
- 广州细胞外基质胶厂家直销 2026-05-18
- 太原细胞外基质胶平均价格 2026-05-18
- 合肥细胞外基质胶平均价格 2026-05-17
- 长沙细胞外基质胶 2026-05-17
- 郑州正规细胞外基质胶进货价 2026-05-17
- 徐州细胞外基质胶 2026-05-15
- 长沙正规细胞外基质胶直销价 2026-05-15
- 贵阳细胞外基质胶报价 2026-05-15
- 宁波珠海细胞外基质胶 2026-05-14
- 济南正规细胞外基质胶厂家 2026-05-14
- 北京正规细胞外基质胶销售厂家 2026-05-14


- 贵阳鼠尾胶原供应商 05-20
- 济南正规鼠尾胶原推荐厂家 05-20
- 宁波鼠尾胶原服务电话 05-20
- 唐山鼠尾胶原厂家供应 05-20
- 唐山正规鼠尾胶原 05-20
- 无锡天津鼠尾胶原 05-20
- 芜湖正规鼠尾胶原销售厂家 05-20
- 正规鼠尾胶原进货价 05-20
- 杭州成都鼠尾胶原 05-20
- 北京鼠尾胶原厂家批发价 05-20