高通量组学技术(如基因组、转录组、蛋白质组)为耐药机制研究提供了系统视角。全基因组测序(WGS)可多方面解析耐药株的突变图谱。例如,对多重耐药结核分枝杆菌的WGS分析发现,rpoB、katG和inhA基因突变分别导致利福平、异烟肼和乙胺丁醇耐药,且突变株在群体中的传播速度明显快于敏感株。转录组学(RNA-seq)则揭示耐药相关的基因表达调控网络。例如,在伊马替尼耐药的慢性髓系白血病细胞中,RNA-seq发现BCR-ABL下游信号通路(如PI3K/AKT、RAS/MAPK)异常开启,且药物外排泵(如ABCB1)表达上调。蛋白质组学(质谱技术)可鉴定耐药相关的蛋白修饰变化。例如,在顺铂耐药的卵巢ancer细胞中,质谱分析发现铜转运蛋白ATP7B表达升高,其通过将顺铂泵出细胞外降低胞内药物浓度,为联合使用铜螯合剂逆转耐药提供了依据。药物筛选技能的研讨与使用。活性筛选成本

环特生物在环肽药物领域构建了多维度筛选平台,涵盖噬菌体展示、mRNA展示及结构导向设计等技术。噬菌体展示技术通过将环肽库展示在病毒表面,结合亲和筛选与扩增循环,可高效识别高亲和力结合物。例如,环特与RatmirDerda实验室合作,利用基于半胱氨酸的环化化学技术,生成了包含光电开关和糖肽的超大环肽库,成功筛选出针对碳酸酐酶(CA)的特异性抑制剂。在结构导向设计方面,环特借鉴Grossmann实验室的研究成果,通过模拟E-cadherin的β-片结构,设计出可抑制Tcf4/β-catenin相互作用的环肽,其IC50值达16μM,为Wnt信号通路相关ancer医疗提供了新候选分子。中药活性筛选高通量筛选特色及使用有哪些?

筛药实验依赖多种技术平台,其中高通量筛选(HTS)是常用的方法。HTS利用自动化设备(如液体工作站、微孔板检测仪)对数万至数百万种化合物进行快速测试,通常结合荧光、发光或比色信号检测靶点活性。例如,基于荧光共振能量转移(FRET)的技术可实时监测酶活性变化,灵敏度高达纳摩尔级。此外,基于细胞的筛选平台(如细胞存活率检测、报告基因分析)能直接评估化合物对活细胞的影响,适用于复杂疾病模型。例如,在神经退行性疾病研究中,可通过检测神经元存活率筛选神经保护药物。近年来,表型筛选(PhenotypicScreening)逐渐兴起,它不依赖已知靶点,而是直接观察化合物对细胞或生物体的整体效应,为发现新靶点提供可能。
药物组合筛选的技术路径主要包括高通量筛选、基于机制的理性设计和计算生物学辅助预测三大方向。高通量筛选通过自动化平台(如微流控芯片、机器人液体处理系统)同时测试数千种药物组合对细胞或模式生物的活性,快速锁定潜在协同对;理性设计则基于疾病分子机制(如信号通路交叉、代谢网络调控),选择作用靶点互补的药物进行组合,例如将EGFR抑制剂与MEK抑制剂联用,阻断肿瘤细胞增殖的多条信号通路;计算生物学方法(如机器学习模型、网络药理学)通过分析药物-靶点-疾病关联数据,预测具有协同潜力的组合,减少实验试错成本。实验设计需严格控制变量,通常采用棋盘滴定法、等效线图法或Bliss单独性模型量化协同效应,并结合统计学分析(如Loewe加和性模型)排除假阳性结果。高通量筛选的意义以及价值有哪些?
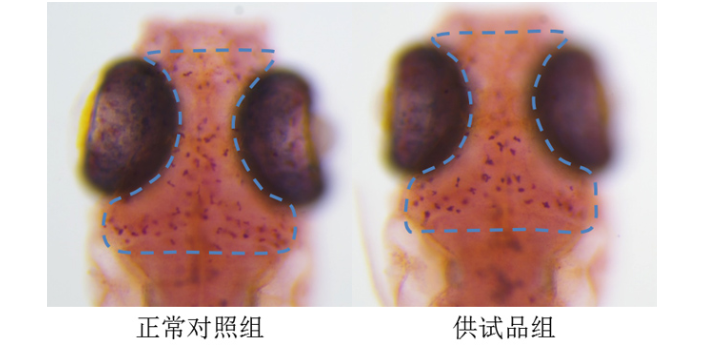
为了确保环特药物筛选结果的可靠性和可重复性,严格的质量控制和标准化流程至关重要。环特建立了一套完善的质量管理体系,从斑马鱼的饲养管理、实验操作规范到数据记录分析,每一个环节都有严格的标准和流程。在斑马鱼饲养方面,严格控制水质、温度、光照等环境条件,保证斑马鱼的健康和一致性。实验操作过程中,对化合物的配制、给药的方式、观察指标等都进行标准化规定,减少人为因素对实验结果的影响。同时,采用先进的仪器设备和数据分析软件,提高实验的准确性和精确性。通过严格的质量控制和标准化,环特药物筛选能够为药物研发提供高质量的数据支持,增强科研成果的可信度和说服力。什么是高通量药物筛选呢?结构生物学药物筛选
用于肿瘤免疫药物高通量筛选渠道有哪些?活性筛选成本
展望未来,环特药物筛选有着广阔的发展前景。随着技术的不断进步,斑马鱼模型将不断完善和优化,能够模拟更多复杂的人类疾病,为药物筛选提供更丰富的实验对象。同时,人工智能和大数据技术的融入将进一步提升药物筛选的效率和精细度,通过对大量实验数据的分析和挖掘,预测化合物的活性和安全性,指导药物研发的方向。然而,环特药物筛选也面临着一些挑战。例如,斑马鱼与人类之间仍存在一定的物种差异,部分实验结果可能无法完全外推到人类。此外,随着药物筛选规模的扩大,对实验资源和数据管理的要求也越来越高。环特需要不断加强技术创新和人才培养,积极应对这些挑战,持续推动药物筛选技术的发展,为人类健康事业做出更大的贡献。活性筛选成本