切片染色的基本原理是利用染料与组织中不同成分之间的亲和性差异,选择性地染色不同的结构或细胞成分。染色过程通常包括几个关键步骤。首先是**固定**,即通过化学药品(如福尔马林)将组织中的细胞成分固定,使其不受外界环境的影响而发生变化。固定后的组织需要通过脱水处理去除水分,再通过透明化处理使其更易于切割成薄片。接下来,通过不同的染色方法,将染料加入到组织中,通常包括酸性染料和碱性染料,它们分别对不同的细胞成分有亲和性,如酸性染料常常染色细胞质,而碱性染料则染色细胞核。***,切片会经过脱水、封片等步骤,以便于长期保存和观察。切片染色的过程虽然复杂,但每个步骤都至关重要,确保了染色效果的准确性和细胞结构的清晰呈现。染色切片可以揭示组织的微观结构和病理变化。番红-固绿染色操作流程
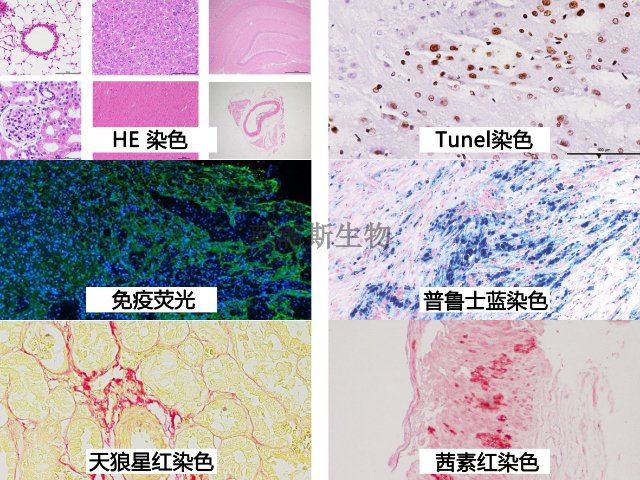
病理切片染色是病理学研究和临床诊断中不可或缺的一环,其目的是通过不同染料与组织成分的特异性结合,使得组织学结构和细胞学细节得以在显微镜下清晰显现。未经染色的组织切片通常呈现无色或浅色,细胞结构难以辨认。通过染色,不同的细胞器、细胞类型以及组织基质会显示出不同的颜色和对比度,从而帮助病理学家识别正常组织与病变组织之间的差异。病理切片染色不仅应用于常规病理诊断,还***用于科研实验中,例如**学、免疫学、神经科学和再生医学等领域。维多利亚蓝染色免疫组化染色可以定位特定蛋白质或抗原。

随着技术的进步,病理切片染色也不断更新。近年来出现的 **多重免疫荧光(mIF)** 和 **多重免疫组化(mIHC)** 技术,使得在同一张切片上检测多个蛋白成为可能。这些方法结合数字病理和图像分析软件,可以对肿瘤免疫微环境进行***解析。此外,**空间转录组学** 和 **成像质谱** 技术的引入,使得病理切片不仅能显示组织形态,还能提供分子层面的空间信息。这些新方法正在推动病理学从传统形态学向多组学整合的方向发展。专业病理染色切片检测拍照平台。
病理染色在动物实验过程中起到一个记录和存档的作用•长期保存:染色后的组织切片可以长期保存,方便以后的研究和参考。•图像记录:通过显微镜拍摄染色后的组织切片图像,可以形成详细的图像记录,便于数据共享和进一步分析。总结病理染色技术在动物实验中具有多重重要作用,不仅能够帮助研究人员详细了解组织的结构和功能,还能检测病变和异常,研究疾病机制,评估药物疗效和毒性,并进行对照研究。这些信息对于推动医学研究、新药开发和临床应用具有重要价值。染色切片是病理层面诊断模型的重要工具。
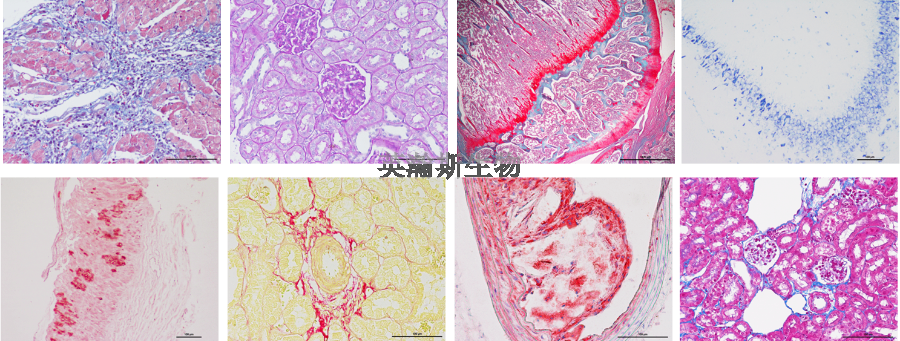
病理切片染色的效果在很大程度上依赖于前期的制备过程。通常包括组织取材、固定、脱水、包埋、切片和脱蜡等步骤。组织固定最常见的是 4% 多聚甲醛或 10% 中性甲醛溶液,能够保持组织结构稳定,防止自溶。石蜡包埋后使用切片机将组织切至 3–5 μm 厚度,再铺展于载玻片上。正式染色前,还需要进行脱蜡和水化,以去除石蜡并恢复组织的亲水性,为后续染色做好准备。如果这些步骤不规范,往往会导致染色不均匀或背景过重,从而影响观察结果。Masson三色染色用于区分肌肉、胶原和纤维组织。维多利亚蓝染色价格
染色切片可以帮助识别病原体。番红-固绿染色操作流程
切片染色的方法有很多,常见的包括**HE染色**、**PAS染色**、**免疫组化染色**等。**HE染色**(Hematoxylin and Eosin Staining)是**为常用的一种染色方法,其中,苏木精(Hematoxylin)主要染细胞核,而伊红(Eosin)则染细胞质。该方法因其操作简便、效果明显而广泛应用于临床组织学和病理学研究。**PAS染色**(Periodic Acid-Schiff Staining)主要用于检测组织中糖类物质的存在,特别是检测糖原、粘多糖等。它通过使组织中的糖类物质与Schiff试剂反应,产生红色或紫色反应,使这些物质在显微镜下非常显眼。对于某些特定的细胞成分,还可以采用**免疫组化染色**,这种方法通过特异性抗体与组织中的抗原结合,使得组织中含有特定蛋白质的区域呈现出不同的颜色,从而有助于研究特定分子的定位和表达。番红-固绿染色操作流程