通过三质粒瞬转体系生产病毒载体,会引入宿主细胞DNA残留(HCD)、蛋白残留(HCP)、工艺杂质(如antibiotics、核酸酶等外源物质)等污染,存在潜在的致瘤性和免疫原性等风险。药品监管机构一般允许生物制品中存在10ng/dose以下的残留DNA。此外,根据杂质来源、工艺以及产品类型不同,也会对HCD限度做不同要求。为了达到这个要求,一般通过核酸酶处理和色谱联用的方法。一般在细胞培养液裂解/收获、澄清收获及超滤浓缩等环节加入核酸酶处理,需要工艺摸索来确认处理方式。黄山高盐核酸酶服务哪家好呢,欢迎咨询上海倍笃生物 。江苏效果高盐核酸酶价格表

基因药物常用的AAV载体有三种生产方法,分别是三质粒瞬转体系、杆状病毒表达载体体系和包装细胞体系。其中,20多年前开发的三质粒瞬转表达技术仍然占据腺相关病毒AAV生产的主流地位,其三质粒分别是Helper质粒(含E2a/b、E4和VARNA基因)、目标基因表达质粒及辅助质粒(含Cap和Rep基因)。虽然AAV病毒载体的血清型不同,但AAV的生产流程基本一致,主要有质粒共转宿主细胞HEK293、293细胞生产病毒颗粒、从细胞培养上清或/及细胞裂解液中收获病毒载体、纯化/制剂/无菌过滤/灌装等流程。河北进口高盐核酸酶价格表SAN HQ高盐核酸酶促进残留DNA的消化,有助于符合FDA要求。
经典的慢病毒载体(LV)的生产工艺如下,——三质粒系统瞬时转染HEK293细胞系,转染24小时后LV由转染阳性细胞生产并排出到培养上清液中;收获上清培养液后,加入核酸酶去除HCD污染,通过澄清步骤去除大的细胞碎片等杂质;下游纯化步骤分离LV载体,纯化方法包括切向流过滤TFF、色谱纯化及超速离心;纯化后的LV病毒颗粒经过无菌过滤,更换到优化后的配方中,灌装并冷冻保存。每批Car-T生产时取对应量的LV病毒,切忌反复冻融,否则LV病毒会失活。
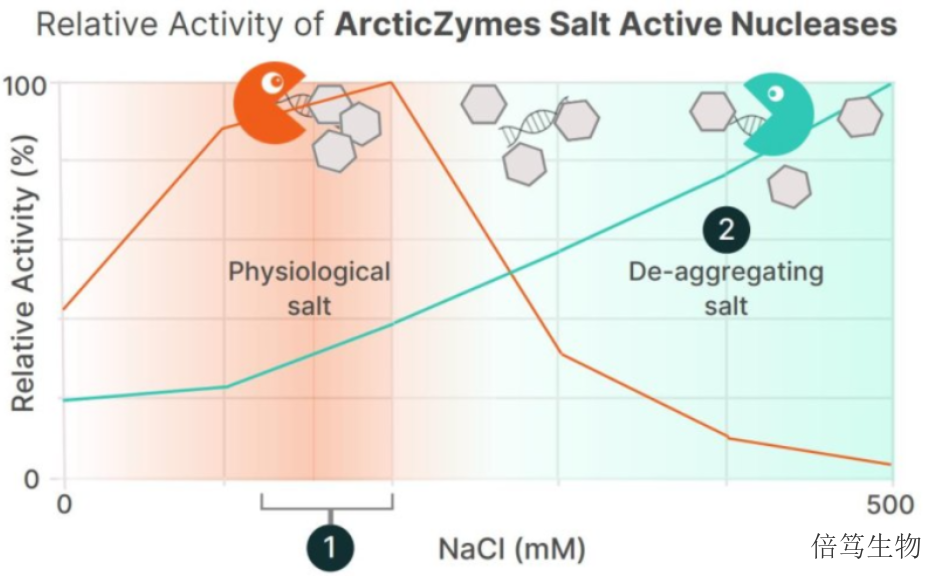
一般来说,生物生产工艺用的核酸酶以BenzonaseTM(BenzonaseTM是Merck的注册商标)为主,能高效降解任何形式(双链、单链、线状、环状)的DNA和RNA。该酶来自于大自然界普遍存在的S.Marcescen,通过E.coli发酵生产得到。该酶的适宜反应条件是低盐浓度范围(<100mM盐浓度),且酶活随着盐浓度上升而下降,在300mM盐浓度时酶活几乎丧失。对于细胞基因药物常用的两种病毒载体LV和AAV,LV由于含有脂包膜结构一般都在生理盐条件下存在,而AAV在高盐条件下不易团聚、更稳定。而在生理盐浓度及更高浓度条件下,Benzonase活性受到抑制。东台高盐核酸酶售后服务哪家好呢,欢迎咨询上海倍笃生物 。
监管部门对HCD的残留量有明确的规定。美国FDA发布的指导原则中指出生物制品HCD残余限度为 100pg/剂,对于大剂量生物制品如单克隆抗体,根据其残留DNA来源及给药途径,残留量可放宽至 10ng/剂。细胞基因药物终产品的DNA残留有两种来源,分别是宿主细胞DNA(HCD)和转染用的质粒。质粒和HCD的存在形式不同,去除效率也差别很大。其中,质粒是裸露的DNA双链,带强负电荷,通过色谱纯化主要是离子交换能够很高效去除;HCD则是以核小体紧密折叠形成的染色质形式存在,几乎不以裸DNA形式存在,所以很难去除。SAN HQ高盐核酸酶有两个级别,分别是生物工艺级别SAN HQ和GMP级别SAN HQ GMP。黑龙江附近哪里有高盐核酸酶联系方式
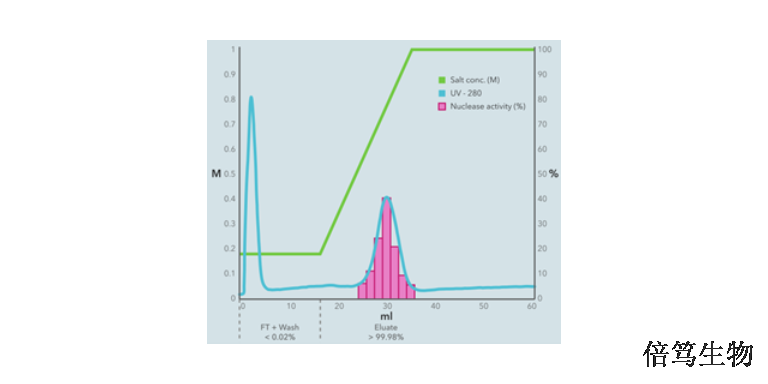
一个美国客户对SAN HQ高盐核酸酶纯化病毒载体的效率进行了评估。江苏效果高盐核酸酶价格表
跟其他类型的核酸酶一样,SAN HQ高盐核酸酶和M-SAN HQ中盐核酸酶的灭活方法有很多,分为可逆灭活及不可逆灭活。金属离子螯合剂如EDTA会可逆抑制两者的活性,加入的EDTA浓度一般是溶液中Mg2+浓度的2倍左右即可完全抑制活性;后续补加过量的Mg2+即可恢复核酸酶活性。加热、还原剂(如DTT)、咪唑、甘油及表面活性剂(如高于15%浓度的Triton X-100、SDS、尿素等)等都可以使其不可逆失活。在生物工艺流程,需要结合上下游应用需要选择合适的方法去除或灭活核酸酶。江苏效果高盐核酸酶价格表