药物组合筛选面临三大关键挑战:一是组合空间性增长(如100种药物的两两组合达4950种,三三组合达161700种),导致实验成本与周期难以承受;二是药代动力学(PK)与药效动力学(PD)的复杂性,不同药物吸收、分布、代谢及排泄的差异可能削弱体内协同效应;三是临床转化率低,只约10%的体外协同组合能在体内验证有效。针对这些挑战,优化策略包括:1)采用智能算法(如机器学习、深度学习)预测潜在协同组合,缩小实验范围。例如,基于药物化学结构、靶点信息及疾病基因组数据构建预测模型,可优先筛选高概率协同组合;2)开发微流控芯片或器官芯片技术,模拟体内动态环境,实时监测药物组合的PK/PD过程,提高体外-体内相关性;3)建立多阶段筛选流程,先通过高通量细胞实验快速筛选,再利用类organ或动物模型验证,进行临床试验,逐步淘汰无效组合,降低研发风险。虚拟筛选在药物发现中的意义。活性成分筛选公司

体内筛选通过构建动物影响或tumor移植模型,更真实地模拟药物在体内的代谢过程及宿主-病原体相互作用。在细菌耐药研究中,小鼠腹膜炎模型是常用体系。例如,将金黄色葡萄球菌接种至小鼠腹腔,随后腹腔注射万古霉素,连续医疗14天后分离肝脏和脾脏中的存活菌株,发现dltABCD基因簇突变导致细胞壁负电荷减少,是万古霉素耐药的重要机制。在tumor耐药领域,患者来源tumor异种移植(PDX)模型因其保留原始tumor的异质性和微环境特征而备受关注。例如,将非小细胞肺ancer患者的tumor组织移植至免疫缺陷小鼠,经奥希替尼医疗8周后,tumor体积缩小50%但后续复发,基因测序显示复发灶中EGFRC797S突变频率从0.1%升至35%,揭示了第三代EGFR-TKI耐药的新机制。小分子化合物药物筛选蛋白质与高通量药物筛选化合物库。
药剂筛选通常包括靶点验证、化合物库构建、筛选模型设计、数据解析与候选化合物优化五个阶段。靶点验证:通过基因敲除、RNA干扰等技术确认靶点与疾病的因果关系,例如验证某激酶在tumor信号通路中的关键作用。化合物库构建:包含天然产物、合成化合物、已上市药物再利用库等,需确保分子多样性和可获取性。例如,某些海洋天然产物因其独特结构成为新型抗菌剂的潜在来源。筛选模型设计:根据靶点类型选择合适的检测方法,如酶活性抑制、细胞信号通路影响或表型变化观察。数据解析:通过统计学方法(如Z-score、IC50计算)筛选活性化合物,并排除假阳性结果。例如,设置多重浓度梯度验证剂量效应关系。候选化合物优化:对初筛阳性化合物进行结构修饰(如引入亲脂基团改善膜通透性)、药代动力学研究(如半衰期、代谢稳定性)及安全性评估(如肝毒性测试),终确定临床前候选药物。例如,某抗糖尿病药物通过结构优化将口服生物利用度从10%提升至60%。
挑选模型建立运用亲本及SOX10-KO细胞作为实验模型,运用CellTiter-Glo®化学发光细胞生机检测办法测定细胞活性,确定先导化合物。分别在0.1μM-10μM浓度下对1820种抗化合物在亲本细胞和SOX10敲除MeWo细胞中进行挑选。结果剖析发现,库中的一切五种cIAP1/2-XIAP抑制剂(LCL161、Birinapant、GDC0152、AZD5582和BV6)可有用诱导SOX10-KO细胞逝世,且对亲代细胞几乎没有影响。所以作者估测,cIAP1和/或cIAP2可能是诱导SOX10敲除细胞逝世的相关靶标。机制探究紧接着,为了验证上述估测,进行了蛋白表达剖析及基因组学剖析,结果表明cIAP2表达与SOX10表达成负相关,cIAP2参加诱导SOX101缺点细胞逝世(图8),并找到了医治RAF和/或MEK抑制剂耐药性的有用计划,即在BRAFi和MEKi计划中加入cIAP1/2抑制剂将延迟获得性耐药的发生。化合物在高通量筛选中的效果怎么样?

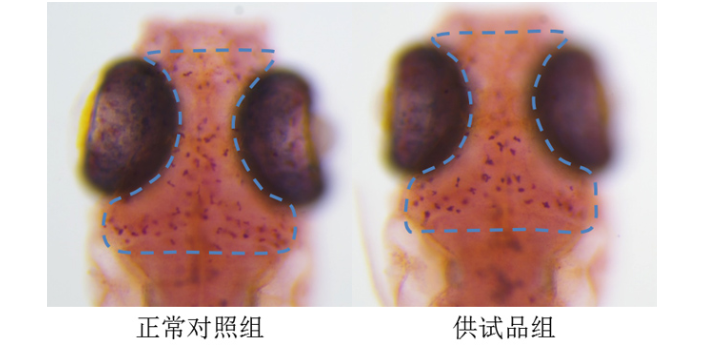
在药物研发的漫漫长路中,环特药物筛选宛如一座明亮的灯塔,为行业指引着高效精细的新方向。传统药物筛选方法往往面临周期长、成本高、成功率低等诸多难题,而环特药物筛选凭借其独特的优势脱颖而出。环特以斑马鱼为模式生物构建筛选体系,斑马鱼具有繁殖能力强、胚胎透明、基因与人类高度同源等特点。这使得科研人员能够在短时间内对大量化合物进行筛选,很大缩短了筛选周期。例如,在筛选抗tumor药物时,利用斑马鱼tumor模型,可快速观察化合物对tumor生长的抑制作用,相比传统动物模型,效率提升数倍。同时,精细的筛选机制能够减少不必要的实验浪费,降低研发成本,让有限的资源集中在更有潜力的药物分子上,为新药研发注入强大动力。高通量筛选的意义以及价值有哪些?药物高通量筛选方法
怎么筛选先导化合物?活性成分筛选公司
高通量组学技术(如基因组、转录组、蛋白质组)为耐药机制研究提供了系统视角。全基因组测序(WGS)可多方面解析耐药株的突变图谱。例如,对多重耐药结核分枝杆菌的WGS分析发现,rpoB、katG和inhA基因突变分别导致利福平、异烟肼和乙胺丁醇耐药,且突变株在群体中的传播速度明显快于敏感株。转录组学(RNA-seq)则揭示耐药相关的基因表达调控网络。例如,在伊马替尼耐药的慢性髓系白血病细胞中,RNA-seq发现BCR-ABL下游信号通路(如PI3K/AKT、RAS/MAPK)异常开启,且药物外排泵(如ABCB1)表达上调。蛋白质组学(质谱技术)可鉴定耐药相关的蛋白修饰变化。例如,在顺铂耐药的卵巢ancer细胞中,质谱分析发现铜转运蛋白ATP7B表达升高,其通过将顺铂泵出细胞外降低胞内药物浓度,为联合使用铜螯合剂逆转耐药提供了依据。活性成分筛选公司