斑马鱼(zebrafish)是一种用于生物学研究的模式生物。它们在多种方面都被用于研究,包含发育、遗传、生理和行为等。其间一个常用的研究办法是运用多孔板试验,它可以用来测验斑马鱼幼鱼的行为和认知才能。多孔板试验是一种基于水迷宫的试验,通常由一个容器、一个多孔板和一些食物组成。试验的过程中,斑马鱼幼鱼被放置在容器中,并被要求经过多孔板来取得食物奖赏。试验的目的是测验斑马鱼幼鱼的学习和记忆才能,以及其对环境的认知才能。斑马鱼实验因其基因与人类高度同源,成为研究人类疾病的重要模型。创新斑马鱼技术

别的还有科学家发现,斑马鱼的脑部神经元较为简单和可猜测。这些研究成果证明了斑马鱼合适用作形式动物。现在咱们已经知道,斑马鱼的基因与人类基因的相似度到达87%,这意味着在其身上做药物试验所得到的结果在大都情况下也适用于人体。此外,雌性斑马鱼可产卵200枚,胚胎在24小时内就可发育成形,这使得生物学家能够在同一代鱼身上进行不同的试验,进而研究病理演化过程并找到病因。正是通过在斑马鱼身上进行的试验,生物学家发现,包含人类在内的一些脊椎动物之所以产下奇异的双头幼仔是因为两种基因活动紊乱形成的。生物模型斑马鱼斑马鱼胚胎透明特性便于观察药物对体内organ影响,省去组织切片步骤,提升实验效率。
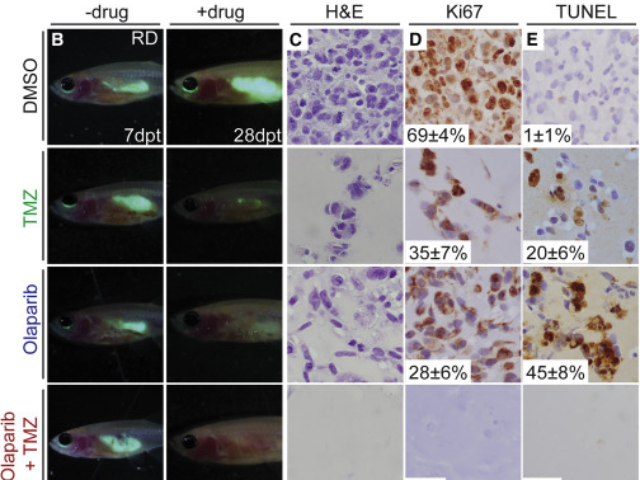
斑马鱼胚胎的透明性与体外受精特性,使其成为发育生物学领域的“活的人体显微镜”。德国马普研究所团队通过单细胞测序技术,绘制出斑马鱼胚胎从受精卵到原肠胚期的细胞命运图谱,揭示了中胚层细胞在背腹轴形成中的动态迁移规律。研究显示,特定转录因子(如Tbx16)通过调控细胞黏附分子表达,引导中胚层前体细胞向预定区域聚集,该机制与小鼠胚胎发育具有保守性,但斑马鱼胚胎因缺乏胎盘屏障,其细胞迁移速度较哺乳动物快到3-5倍。在基因编辑技术赋能下,斑马鱼成为研究organ发生的理想模型。哈佛大学团队利用CRISPR-Cas9技术,在斑马鱼胚胎中同时敲除多个心脏发育相关基因(如gata4、nkx2.5),发现其心脏原基在原肠运动阶段即出现融合缺陷,较传统小鼠模型提前48小时暴露表型。更突破性的是,通过光遗传学工具调控特定神经嵴细胞活性,可实时观察心脏瓣膜发育过程中细胞命运的可塑性,揭示了心脏畸形中“基因-细胞-组织”的多级调控网络。这些发现为先天性心脏病早期干预提供了新的分子靶点。
令人惊奇的是,这种生活在热带的鱼还可以“再造”被部分切除的组织,从而为从事修正受损脊髓的研讨人员打开了方便之门。现在,斑马鱼的使用正逐渐拓宽和深化到生命体的多种系统的发育、功用和疾病的研讨中,并用于遗传学、药物学、毒理学等诸多方面。在药品研发等方面,每年有很多新药进入临床或者临床前阶段,它们是否对人体有害需要进行科学的安全点评。“实验新星”斑马鱼再次担当重担,斑马鱼胚胎和幼鱼对有害物质十分敏感,同时用药简单,只需将药物放入养殖胚胎的水中或快速打针,用药量少、测验周期短。斑马鱼与基因编辑在脑科学研究的应用。
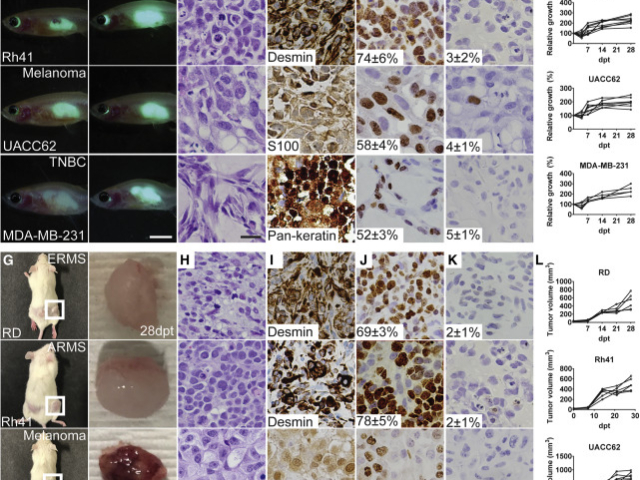
【试验计划】咱们将受测试斑马鱼分成两组,分别是正常对照和服用/打针供试品组(供试品经过溶解到养鱼用水中或打针的方法摄入到斑马鱼体内)。服用/打针药物一段时间后,检测尾长、彗星长、尾矩和Olive尾矩。能够看到,服用/打针供试品组斑马鱼细胞核呈现拖尾。该供试品改变DNA链的负超螺旋结构、空间构象,使DNA链断裂、形成类核,终究导致细胞逝世(坏死、凋亡或自体吞噬)。【点评结论】1.经过每组30尾斑马鱼的比照试验,服用/打针供试品组的斑马鱼细胞核呈现显着拖尾,与正常对照组存在显着的差别。2.本试验证明了该供试品对斑马鱼有基因毒性。斑马鱼幼鱼孔板实验需严格控制温度、光照及水质,确保实验数据准确可靠。斑马鱼实验室系统预算
斑马鱼旷场实验通过分析运动轨迹,评估药物对行为及神经系统毒性的影响。创新斑马鱼技术
因此在科学家和研讨中将它用于药物研发,用它来发展生物学,遗传学,乃至是环境科学,布里斯托研讨人员将花费五年时刻寻找与伤疤构成相关的基因,这将包含非凡斑马鱼的实时成像和遗传分析,假如去除,鱼可以长出尾鳍并敏捷修正任何伤口,研讨小组还将研讨伤疤患者的组成和遗传改变。据了解,英国有2000万人身上留下令人头疼的伤痕,现已对日子造成了影响,伤疤的存在会引起长期的情绪和身体问题,包含痛苦,瘙痒和行动不便,需求常常进行手术,植皮,每天屡次涂抹乳霜和进行理疗。创新斑马鱼技术