子宫内膜异位症模型异位灶的形成需要有血管的建立来提供能量。血管内皮细胞因子(VEGF)是一种多功能的细胞因子,它可促进血管内皮细胞增殖。黄荷凤[口]将EM患者的子宫内膜种植到ICR小鼠腹腔内,移植后3d内,移植的内膜细胞只能够通过腹腔液或者临近组织得到部分的氧和营养物质,所以受到了缺血缺氧等的剌激,从而诱导了VEGF的强表达,使它明显高于手术前,通过诱导血管形成及组织重构来满足继续生长。VanLangendonckt[四]等将月经期内膜加入血清或红细胞接种于裸鼠腹腔,观察到间质中含铁血黄素沉积。认为经血中红细胞是形成含铁血黄素的原因,也是引起慢性炎症和氧化损伤的因素之一,从而诱导VEGF等的表达,通过促使新生血管的形成参与了EM的病理通过子宫内膜异位症模型,我们可以研究疾病对女性生活质量的影响。广东大鼠子宫内膜异位症模型实验外包
(1)自发性模型的建立常见于人或灵长动物,其病理学特征及病机和人类比较为相似,但发生率低,周期长,短期内无法获得足够的信息,且价格昂贵,限制了其在科研中的应用。(2)移植性多见于SCID小鼠或裸小鼠,有同种异体和异种异体之分,均有创伤小、易操作、成活率高等优点。SCID小鼠是严重联合免疫缺陷小鼠,为先天性T、B淋巴细胞联合免疫缺陷动物,用其进行移植后成活率较裸小鼠高,国外已将SCID小鼠作为人子宫内膜组织的受体动物。但是由于实验动物免疫缺陷动物,无法用于子宫内膜异位症免疫学机制及免疫改善方面的研究。美迪西根据客户的需求提供各种有效的动物模型,用来检测药物的有效性,实验动物有非人类灵长动物、狗、小鼠、大鼠、家兔、豚鼠、裸鼠等各种种类。(3)诱发性也为自体移植,其造模对象较广,如猴、兔、大鼠等。将其自体内膜通过手术种植到宫腔外,或闭锁其宫颈,使经血逆流而诱发。此法避免了排斥反应,但自体手术移植损伤大且死亡率高。江西子宫内膜异位症模型如何构建该模型为子宫内膜异位症的临床研究提供了有力的支持。
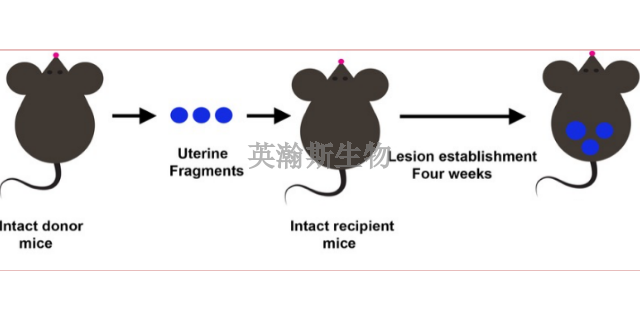
通过建立子宫内膜异位症模型,我们可以更普遍地了解这一复杂疾病的发展过程。这一模型为我们提供了一个模拟真实人体环境的平台,使得我们能够在实验室中精确地模拟子宫内膜异位症从初始病变到逐渐恶化的全过程。通过观察模型中的病理变化,我们可以深入剖析疾病的发病机制,从而更加准确地把握其发展规律。此外,子宫内膜异位症模型还有助于我们研究疾病在不同阶段的特点和表现,为疾病的早期发现和精细改善提供有力支持。因此,通过建立子宫内膜异位症模型,我们能够更深入地了解疾病的发展过程,为临床诊断和改善提供更为科学的依据。
子宫内膜异位症模型的观察指标验证模型是否成功:大鼠建模28d后再次手术,腹腔麻醉后固定,腹部备皮,消毒铺巾,取原切口旁开腹,取出3个不同部位的移植物。记录移植物大体特点。用游标卡尺测量移植物的长度、高度与宽度,按公式计算体积:体积=0.52×长×宽×高[4]。用电子天平称取移植物质量。将取出的移植物和左侧子宫的在位内膜标本用10%多聚甲醛固定,常规石蜡包埋,H-E染色,显微镜下观察组织病理学变化来验证模型的成功率。子宫内膜异位症模型为疾病的早期诊断提供了可能性。
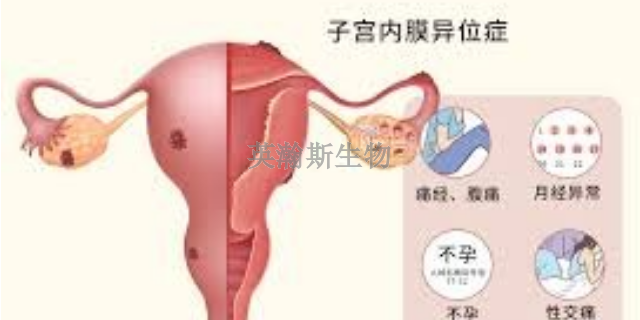
子宫内膜异位症模型的建立无疑为生殖健康领域的进步注入了新的动力。这一模型的精细模拟与高度仿真,使得研究人员能够更深入地了解子宫内膜异位症的发病机理、病理过程及其对生殖系统的影响,从而为疾病的预防、诊断和改善提供了更为科学的依据。同时,该模型也为生殖健康领域的研究人员提供了一个全新的实验平台,有助于加速相关研究成果的转化与应用。因此,可以说子宫内膜异位症模型的建立,不仅为疾病研究提供了重要的工具,更推动了生殖健康领域的快速发展,为广大女性的健康福祉贡献了力量。研究人员正在利用子宫内膜异位症模型探索疾病的微生态失衡问题。陕西专业的子宫内膜异位症模型实验外包
子宫内膜异位症模型为药物研发提供了重要的实验平台。广东大鼠子宫内膜异位症模型实验外包
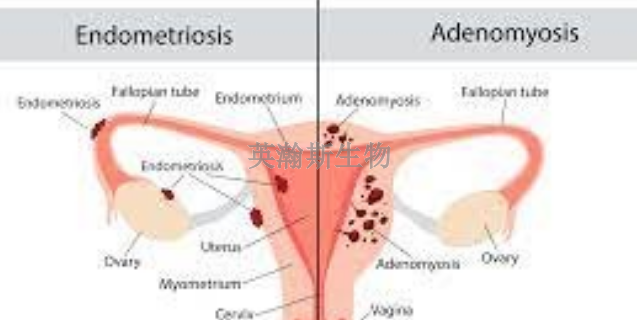
子宫内膜异位症(endometriosis,EM)是一种因子依赖性的常见良性变化,多发于生育年龄妇女,其发病率为10%-159毛。迄今为止,关于EM的真正发病机制并未比较终阐明,且缺少有效的治疗方法。其中一个主要原因是这种疾病只发生于人类和灵长类动物。由于实际操作和伦理学方面的约束,严重限制了对该疾病的研究,因此需要一种可在实验动物体内复制该病的方法。1922年Jacobson初次建立了兔的EM模型,从而开创了EM研究的新局面。本文就EM模型建立、应用的现状及进展进行综述。广东大鼠子宫内膜异位症模型实验外包